Jednostka Badawcza DPL – Cytotoksyczność – Metoda dyfuzji agaru ISO 10993 – 5
Metoda dyfuzji agaru przedstawiona w normie ISO 10993 część 5 jest jedną z metod badania cytotoksyczności in vitro poprzez pośredni kontakt badanego materiału z agarem. Procedura wykorzystywana jest do biologicznej oceny wyrobów medycznych z wykorzystaniem linii komórkowej L-929.
 Postępowanie zgodnie z procedurą opracowaną na podstawie ISO 10993 „Biologiczna ocena wyrobów medycznych – część 5: Badania cytotoksyczności in vitro” pozwala na jakościową ocenę cytotoksyczności badanego materiału tj. wyrób medyczny. Metoda nie jest odpowiednia dla uwalnianych substancji, które nie mogą dyfundować przez warstwę agaru lub które mogą reagować
Postępowanie zgodnie z procedurą opracowaną na podstawie ISO 10993 „Biologiczna ocena wyrobów medycznych – część 5: Badania cytotoksyczności in vitro” pozwala na jakościową ocenę cytotoksyczności badanego materiału tj. wyrób medyczny. Metoda nie jest odpowiednia dla uwalnianych substancji, które nie mogą dyfundować przez warstwę agaru lub które mogą reagować
z agarem.
Procedura badania efektu cytotoksycznego in vitro metodą dyfuzji agaru wg normy ISO 10993 część 5 przeprowadzana jest w laboratorium komórkowym. Polega na wyłożeniu agaru z medium komórkowym na warstwę komórek linii L-929 o odpowiedniej konfluencji. Na górną warstwę agaru przykładany jest badany materiał. Całość inkubowana jest przez 24 – 26 godziny w temperaturze 37 ± 1°C oraz w warunkach 5 ± 1% CO2. Rysunek 1 prezentuje wygląd dołka płytki hodowlanej, gdzie na samym dole znajdują się komórki, następnie agar z medium komórkowym na który umieszczany jest badany materiał.
Odczyt wpływu cytotoksycznego następuje po dobie inkubacji badanego materiału z komórkami oraz agarem. Należy wówczas ocenić pod mikroskopem stan komórek bezpośrednio przed i po usunięciu badanego materiału w oparciu o opisowe wytyczne zawarte w normie ISO 10993 – 5.
Biologiczną ocenę wyrobu medycznego pod kątem wpływu cytotoksycznego na komórki wydaje się na podstawie obserwacji stanu komórek pod mikroskopem. Efekt cytotoksyczności badanego materiału na linię komórkową określany jest na podstawie skali, gdzie 0 oznacza brak wpływu badanego materiału na komórki, a 4 oznacza poważną reakcję cytotoksyczną in vitro. Uzyskanie oceny liczbowej większej niż 2 (łagodna reakcja), w oparciu o wytyczne z normy ISO 10993 – 5, oznacza działanie cytotoksyczne badanego wyrobu medycznego.
Badanie cytotoksyczności metodą pośredniego kontaktu taką jak dyfuzja agaru jest potwierdzoną procedurą testową. Może jednak nie być akceptowana przez wszystkie jednostki regulacyjne.
Zapraszamy do bezpośredniego kontaktu w celu wybrania odpowiedniej metody badawczej dla wyrobu medycznego.
Nasze laboratorium posiada certyfikat Dobrej Praktyki Laboratoryjnej w części biokompatybilność (zakres 9) dla biologicznej oceny wyrobów medycznych dla badań m.in. cytotoksyczności in vitro.
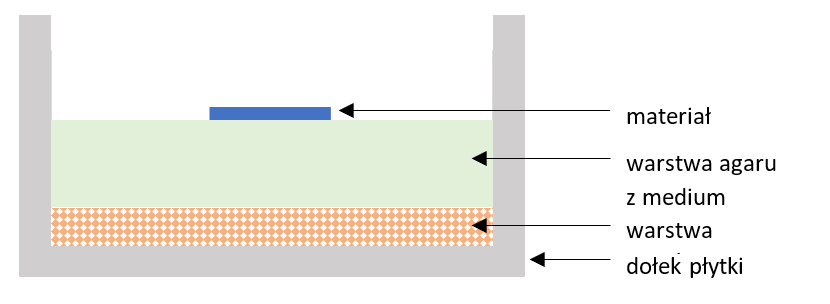
Rysunek 1 Wizualizacja dołka płytki hodowlanej w badaniu cytotoksyczności metodą dyfuzji agaru zgodnie z ISO 10993 „Biologiczna ocena wyrobów medycznych – część 5: Badania cytotoksyczności in vitro”.












